シリコンの酸化膜:構造と不純物拡散
シリコン酸化膜の重要性
今日、半導体デバイスのほとんどがシリコンから作られています。この理由の一つは、化学的に安定かつ絶縁性の高い酸化膜(SiO2)が容易に形成可能なためです。
半導体デバイスにおいて、酸化膜の活用例は以下の通りです。
- 素子間の絶縁分離
- ゲート絶縁膜
- 不純物保護膜
- マスク用絶縁膜
- 表面パッシベーション
このように、半導体デバイスにおいてはSiO2が絶縁膜や保護膜として多用されています。
ここでは、シリコン酸化膜の中でも、最も一般的で多用されるシリコン熱酸化膜について解説します。
なお、こちらの解説は先人たちの名著:半導体シリコン結晶工学を大いに参考にさせていただいております。興味がある方はぜひご参照してください。
熱酸化膜の構造
二酸化ケイ素(SiO2)には様々な結晶多形が存在します。結晶相としては10種類以上、非晶質としては3種類以上が報告されています。
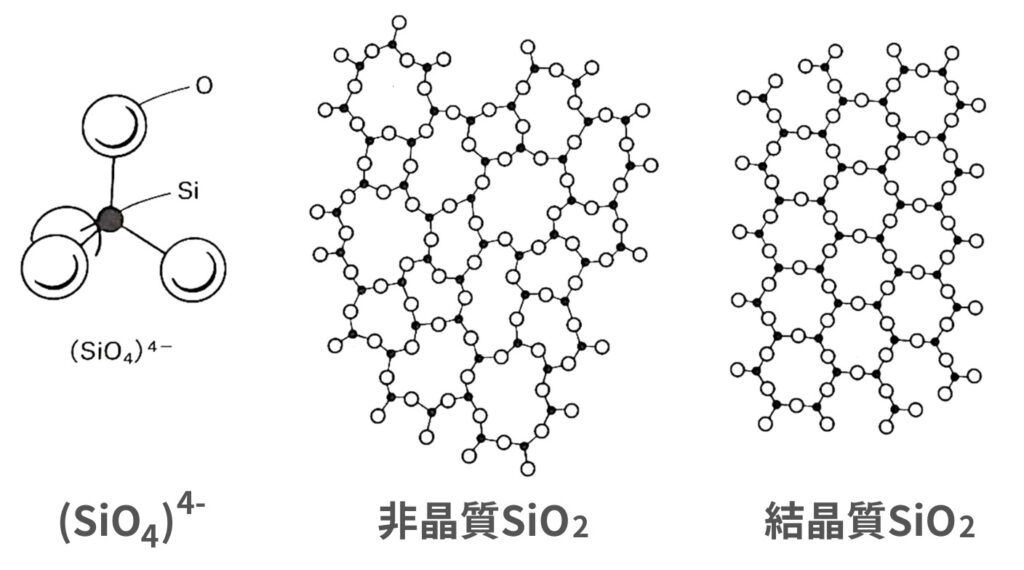
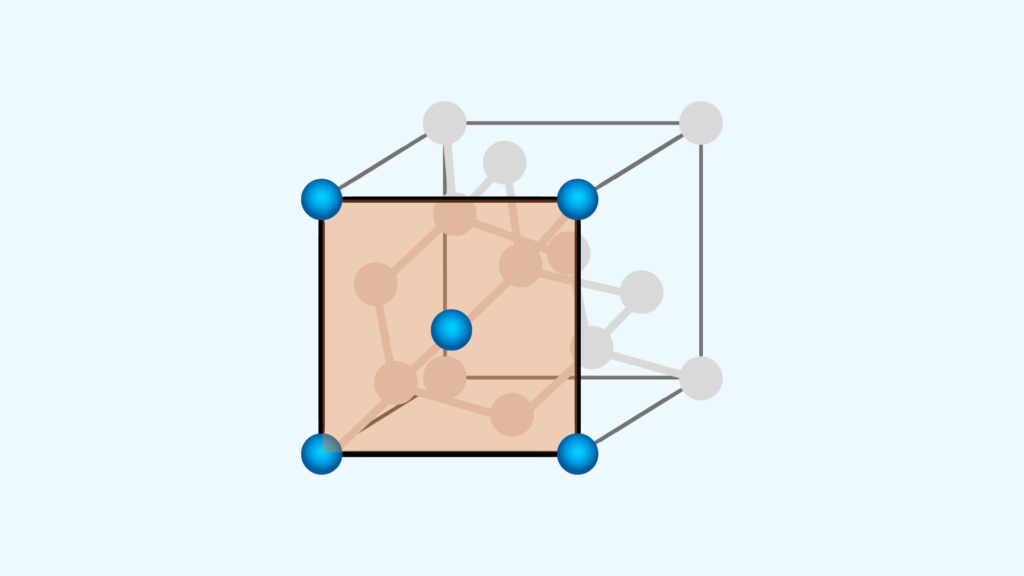
下図は、SiO2を構成する基本単位である、(SiO4)4-正四面体、非晶質SiO2、結晶質SiO2の構造です。
二酸化ケイ素では、非晶質・結晶質に因らず(SiO4)4-正四面体が基本構造になっています。この四面体の中心にはSi4+が存在し、各頂点に4つのO2-が結合しています。
非晶質SiO2では、(SiO4)4-四面体の各頂点酸素を共有することで、3次元網目構造を形成しています。このときの頂点酸素を架橋酸素(bridging oxygen)と呼びます。四面体同士の結合角は規定されないため、非晶質SiO2の構造はランダムなものとなります。
一方、結晶質SiO2の場合には、(SiO4)4-が規則正しく並んだ3次元網目構造となります。
シリコン熱酸化膜は「非晶質SiO2」であることが知られています。
非晶質SiO2であるシリコン熱酸化膜の性質は、酸化条件やSi基板の性質などに依存します。
N.W.FとN.W.M.
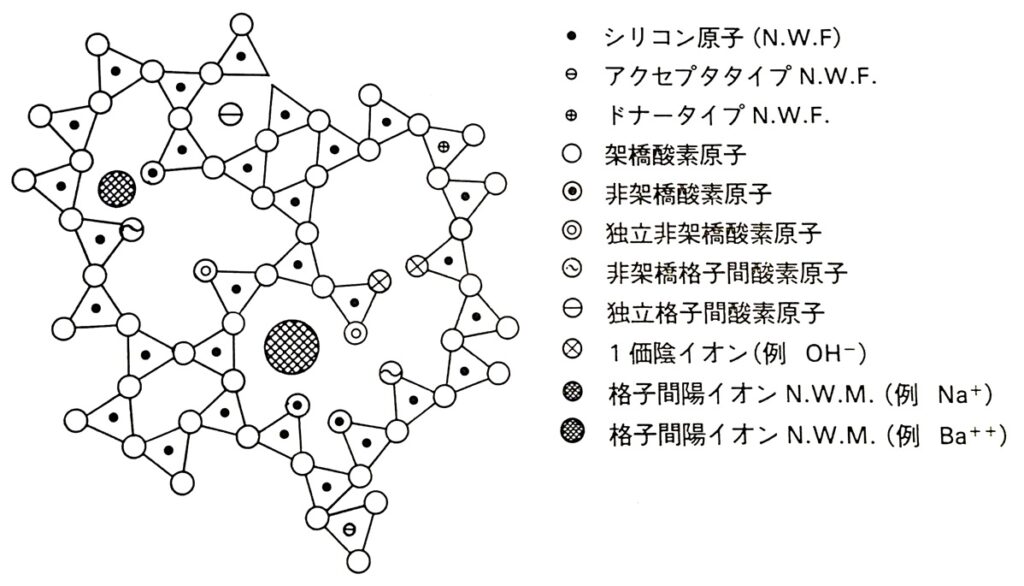
理想的な熱酸化膜(非晶質SiO2)は3次元網目構造であることを述べました。しかし、実際の熱酸化膜中には不純物や欠陥が導入されます。
シリコン結晶中の不純物と同じように、SiO2中の不純物も、
- 格子位置不純物
- 格子間位置不純物
の2つに大別されます。中でも、陽イオン不純物については
- 格子位置の陽イオン不純物=網目形成イオン(N.W.F.)
- 格子間位置の陽イオン不純物=網目修飾イオン(N.W.M.)
と呼びます。
ある陽イオンがN.W.F.またはN.W.M.となるかは、そのイオンと酸素イオンの半径比、酸素配位数、結合力などによって決定されます。
より直接的には、陽イオンと酸素イオン間の静電的引力(CFS, cationic field strength)の大きさによって決まり、以下の式で計算されます。
$$CFS = \frac{2z}{a^2}$$
z:陽イオンの価数、 a:陽イオン-酸素間距離
「CFSが大きい=陽イオンと酸素イオン間の結合力が強い」を意味します。すなわち、CFSが大きいほど結合を形成しMO4四面体を形成しやすいため、N.W.F.となります。
下表はN.W.F.、N.W.M.の一覧です。
| 陽イオン | 電気陰性度 | 陽イオン・酸素イオン間の静電的引力(CFS) (2z/a2) | 備考 |
|---|---|---|---|
| P5+ | 2.1 | 4.30 | 完全なN.W.F. |
| B3+ | 2.0 | 3.22 | |
| As3+ | 2.0 | 3.20 | |
| Si4+ | 1.8 | 3.14 | |
| Ge4+ | 1.8 | 2.65 | |
| Sb3+ | 1.8 | 2.66 | |
| Ti4+ | 1.6 | 2.08 | 通常はN.W.F. |
| Sn4+ | 1.7 | 1.89 | |
| Al3+ | 1.5 | 1.69 | |
| Zr4+ | 1.6 | 1.55 | |
| Fe3+ | - | 1.57 | N.W.F.とN.W.Mが共存 |
| Be2+ | 1.5 | 1.51 | |
| Mg2+ | 1.2 | 0.95 | |
| Ni2+ | - | 0.95 | |
| Zn2+ | - | 0.91 | |
| Co2+ | - | 0.91 | |
| Fe2+ | - | 0.87 | |
| Pb2+ | - | 0.53 | 通常はN.W.M. |
| Ca2+ | 1.0 | 0.69 | 完全なN.W.M. |
| Sr2+ | 1.0 | 0.58 | |
| Ba2+ | 0.9 | 0.51 | |
| Li+ | 1.0 | 0.45 | |
| Na+ | 0.9 | 0.35 | |
| K+ | 0.8 | 0.27 | |
| Rb+ | 0.8 | 0.24 | |
| Cs+ | 0.7 | 0.22 |
シリコンのドーパントとして使用されるP,B,As,Sb,AlはすべてN.W.Fです。一方、価数が小さく、イオン半径が大きいことから、酸素との結合力の弱いLi,Na,K,Csなどのアルカリ金属やアルカリ土類金属はN.W.M.です。表より、N.W.M.となる陽イオンは3,4,5価と価数の高い陽イオンであることが分かります。
酸化膜中の不純物拡散
シリコン熱酸化膜(非晶質SiO2)は隙間の多い開放的な構造を有するにも関わらず、「ドーパントや金属不純物に対して優れた拡散障壁になる」ことが知られています。
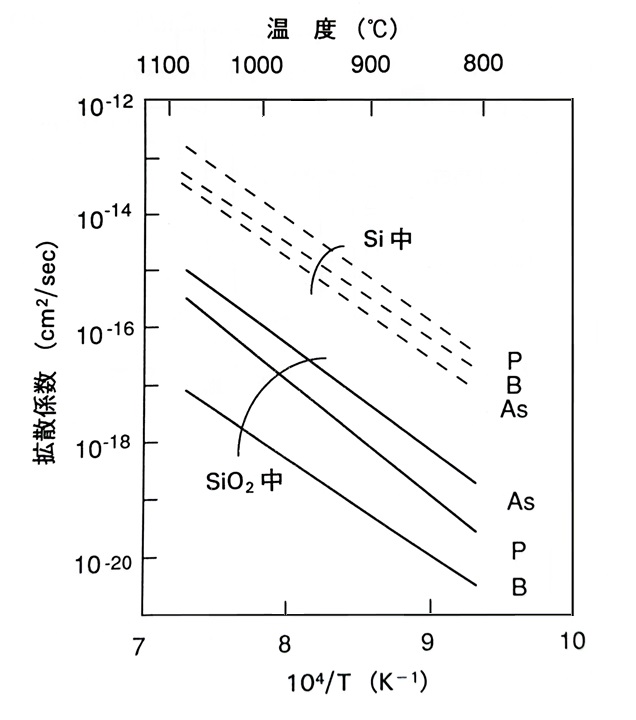
下図はSi中およびSiO2中の各種ドーパントの拡散係数の温度依存性です。
ドーパントや金属不純物のシリコン酸化膜中の拡散係数は、シリコン基板中と比較し、約2-3桁小さいことが知られています。
理由は、ドーパントや金属不純物はN.W.F.やN.W.M.として非晶質SiO2中の構造に取り込まれるためです。この特性から、シリコン熱酸化膜は不純物保護膜に使用されています。
物質の拡散係数Dは下式で表されます。
$$D = D_0 \exp(\frac{-Q_0}{kT})$$
D:拡散係数、 D0:拡散定数、 Q0:活性化エネルギー、 k:ボルツマン定数、 T:温度
拡散定数D0と活性化エネルギーQ0は、1/Tに対してlnD0をプロットするアレニウスプロットから求められます。
また、不純物濃度が表面(x=0)で一定値(C<0)であり、無限厚さのSiウェハーに拡散する場合(一次元拡散の不純物濃度分布は下式で表されます。
$$C(x,t)=C_0 \times erfc(\frac{x}{2\sqrt{Dt}})$$
C(x,t):位置x,時間tにおける不純物濃度、 C0:表面不純物濃度、 erfc:エラー関数の補関数、 x:表面からの距離、 D:拡散係数、 t:時間
上式から、表面濃度C0、拡散係数Dが一定条件下の、時間t、深さxにおける不純物濃度が算出可能です。また、√(Dt)を拡散距離と呼びます。
以下は、SiO2中の各物質の拡散定数と1時間当たりの拡散長の一覧です。
| 拡散種 | D0 [cm2/s] | Q0 [eV] | 拡散長L [μm] | |||
|---|---|---|---|---|---|---|
| 1100℃ | 1000℃ | 900℃ | 800℃ | |||
| B | 1.7×10-5 | 3.37 | 1.6×10-3 | 5.2×10-4 | 1.4×10-4 | 3.0×10-5 |
| P | 1.9×10-2 | 4.03 | 3.3×10-3 | 8.6×10-4 | 1.8×10-4 | 2.8×10-5 | As | 6.7×101 | 3.70 | 7.8×10-1 | 2.3×10-1 | 5.4×10-2 | 9.9×10-3 | O2 | 2.7×10-4 | 1.16 | 7.3×101 | 5.0×101 | 3.2×101 | 1.9×101 | H2 | 5.7×10-4 | 0.45 | 2.1×103 | 1.8×103 | 1.5×103 | 1.5×103 | H2O | 1.0×10-6 | 0.79 | 2.1×101 | 1.6×101 | 1.2×101 | 8.3×100 | Na | 3.4×10-2 | 1.22 | 6.4×102 | 4.2×102 | 2.6×102 | 1.5×102 | S | 6.0×10-5 | 2.6 | 7.7×10-2 | 3.3×10-2 | 1.2×10-2 | 3.6×10-3 | Au | 8.5×103 | 3.7 | 8.8×100 | 2.6×100 | 6.1×10-1 | 1.1×10-1 |
(出典:半導体シリコン結晶工学を元に筆者作成)
B, P, Asといったドーパントの拡散係数・拡散長が小さいことが分かります。
一方で、H2、O2、H2Oといった拡散種の拡散係数・拡散長は酸化膜中でも比較的大きい事もわかります。
シリコンの熱酸化は、表面から内部に進行していくため、表面の酸化種(H2、O2、H2Oなど)が酸化膜を拡散し、SiO2/Si界面に到達する必要があります。これら酸化種の、酸化膜中の拡散係数が高いことから、シリコンの熱酸化は容易に進行するのです。
前の講座
次の講座